
Estela Zimmer Cardoso1; Chrystian Nunes Gonçalves2; Gabriel Valim Cardoso3
DOI: 10.5935/2595-170X.20250032
RESUMO
OBJETIVO: Analisar a literatura sobre biomateriais aplicados à cicatrização de queimaduras, a fim de sintetizar os achados e fundamentar teoricamente o potencial de uma membrana nanocompósita bioativa e multifuncional.
MÉTODO: Revisão narrativa da literatura voltada à análise dos tratamentos atuais e das propriedades de biomateriais aplicáveis à cicatrização de feridas.
RESULTADOS: Os tratamentos atuais apresentam limitações quanto à eficácia, custo e aplicabilidade. A análise das propriedades dos biomateriais sugere que a sinergia entre álcool polivinílico (PVA), nanofibrilas de celulose (NFC) e ácido tânico (TA), proposta teoricamente nesta revisão, pode constituir uma possível plataforma curativa bioativa e multifuncional.
CONCLUSÕES: A fundamentação teórica indica que a membrana, proposta a partir da hipótese da sinergia dos componentes, seria biocompatível, flexível e resistente, poderia manter um ambiente úmido ideal, absorver o excesso de exsudato, apresentar propriedades antimicrobianas e antioxidantes, além de permitir liberação controlada de fármacos e possuir capacidade autorregenerativa. Apesar dos resultados apresentarem uma base teórica para a formulação prática da membrana, são necessários estudos experimentais para validar suas propriedades físicas, químicas, além de eficácia clínica e segurança.
Palavras-chave: Queimaduras. Materiais Biocompatíveis. Cicatrização. Nanocomposto. Taninos.
ABSTRACT
OBJECTIVE: To analyze the literature on biomaterials applied to burn wound healing, in order to synthesize the findings and provide a theoretical foundation for the potential of a bioactive and multifunctional nanocomposite membrane.
METHODS: Narrative review of the literature focused on the critical analysis of current treatments and the properties of biomaterials relevant to wound healing.
RESULTS: Current treatments show limitations regarding efficacy, cost, and applicability. The analysis of biomaterial properties suggests that the synergy between polyvinyl alcohol (PVA), cellulose nanofibrils (NFC), and tannic acid (TA), as theoretically proposed in this review, may constitute a possible bioactive and multifunctional healing platform.
CONCLUSIONS: Theoretical analysis suggests that the proposed membrane, based on the hypothesis of synergistic components, would be biocompatible, flexible, and mechanically stable. It could maintain an optimal moist environment, absorb excess exudate, provide antimicrobial and antioxidant activity, and allow for controlled drug release and self-healing capabilities. Although these findings provide a theoretical basis for the membrane's practical formulation, experimental studies are required to validate its physical and chemical properties, as well as its clinical efficacy and safety.
Keywords: Burns. Biocompatible Materials. Wound Healing. Nanocomposites. Tannins.
INTRODUÇÃO
Embora o tratamento de queimaduras tenha evoluído ao longo do tempo, existem desafios importantes a serem solucionados para uma terapia eficaz. Os curativos tradicionais, como a gaze impregnada com sulfadiazina de prata, estão associados a trocas dolorosas, toxicidade celular e prolongamento do tempo de cicatrização. Abordagens mais modernas, como hidrocoloides, hidrogéis, espumas, alginatos e xenoenxertos, apresentam vantagens, mas muitas vezes não atendem simultaneamente às exigências clínicas ideais, como controle da infecção, absorção adequada de exsudato, manutenção da umidade e custo acessível1.
Nesse contexto, há crescente interesse no desenvolvimento de biomateriais com propriedades multifuncionais, visando à criação de um curativo ideal que atenda às diversas necessidades da cicatrização de queimaduras. O álcool polivinílico (PVA) destaca-se como polímero hidrossolúvel, biocompatível e de baixo custo, mas com limitações, como baixa resistência mecânica e ausência de ação antimicrobiana inerente2. A adição de nanofibrilas de celulose (NFC), de origem vegetal e sustentável, confere maior resistência estrutural e elevada capacidade de absorção de exsudatos3,4. Já o ácido tânico (TA), um polifenol natural, possui comprovada ação antimicrobiana, antioxidante e a capacidade de formar redes reticuladas estáveis com o PVA4-6.
Portanto, este artigo realiza uma revisão crítica dos tratamentos atuais para queimaduras e das propriedades de biomateriais para, a partir dessa análise comparativa, sintetizar os achados e fundamentar teoricamente o potencial de uma membrana nanocompósita - material formado por uma matriz polimérica com partículas nanométricas dispersas - autorregenerativa, com potencial bioativo e capacidade de liberação controlada de fármacos, baseada na combinação sinérgica de PVA, NFC e TA.
MÉTODO
Trata-se de uma revisão narrativa da literatura voltada à análise de biomateriais aplicáveis ao tratamento de queimaduras.
Foi realizada uma busca abrangente nas bases de dados PubMed/MEDLINE, SciELO e Google Scholar, utilizando os seguintes Descritores em Ciências da Saúde (DeCS) e seus correspondentes no Medical Subject Headings (MeSH): "queimaduras" (burns), "bandagens" (bandages), "álcool de polivinil" (polyvinyl alcohol), "celulose" (cellulose), "taninos" (tannins), "hidrogéis" (hydrogels), "nanogéis" (nanogels), "materiais biocompatíveis" (biocompatible materials), "sistemas de liberação de medicamentos" (drug delivery systems).
Para ampliar a sensibilidade da busca, foram utilizadas as seguintes palavras-chave e suas variações: "curativo" (wound dressing), "membrana" (membrane) "nanocompósito" (nanocomposite), "nanofibrilas de celulose" (cellulose nanofibrils) e "ácido tânico" (tannic acid).
Os critérios de inclusão foram: artigos de revisão, metanálises, ensaios clínicos, estudos experimentais in vitro e in vivo e teses acadêmicas que abordassem diretamente o tratamento de queimaduras, o desenvolvimento de curativos, as propriedades de biomateriais (especificamente PVA, nanocelulose e ácido tânico), a cicatrização de feridas e a engenharia de tecidos. Livros e endereços eletrônicos de associações governamentais foram utilizados como complemento à pesquisa. A seleção das fontes foi guiada pela relevância temática, qualidade científica e aplicabilidade clínica. Os materiais selecionados foram lidos na íntegra e as informações relevantes extraídas de acordo com os temas de interesse.
RESULTADOS
A partir da metodologia de busca e dos critérios de seleção de artigos, 78 artigos foram selecionados no total. Inicialmente, 45 artigos foram incluídos como referências, mas, após uma seleção final priorizando os estudos mais recentes e com maior relevância para o tema, 30 artigos foram utilizados diretamente no texto. Esta seção apresenta os resultados baseados na revisão da literatura científica atual. Primeiramente, é necessária uma avaliação crítica e comparativa dos tratamentos atualmente disponíveis para queimaduras, a fim de estabelecer um panorama de suas vantagens, desvantagens e das lacunas que justificam o desenvolvimento de uma nova abordagem.
Tratamentos atuais
A complexidade e a heterogeneidade inerente das feridas por queimaduras exige diferentes abordagens de acordo com a gravidade, profundidade, presença de infecção, quantidade de exsudato, entre outras características a serem consideradas.
Desse modo, devido à carência de um tratamento único para todos os tipos de feridas, alguns materiais com propósitos diferentes foram desenvolvidos e aplicados ao longo das décadas, cada qual com suas vantagens e desvantagens, conforme sintetizado na Tabela 1.
O curativo ideal
A análise dos tratamentos, apresentada na seção anterior, revela que, apesar das opções disponíveis, nenhum curativo consegue, isoladamente, atender a todas as complexas demandas do leito de uma queimadura. Diante desse cenário, para o desenvolvimento de novas tecnologias que supram essas necessidades sem apresentar desvantagens significativas, é preciso consolidar, com base na fisiologia da cicatrização e nas evidências clínicas, as características fundamentais que constituem um curativo considerado ideal para o tratamento de queimaduras.
Tradicionalmente, a cicatrização de feridas é dividida em quatro fases: hemostasia, inflamação, proliferação celular e remodelação. No contexto das queimaduras, a fase de inflamação é especialmente delicada, visto que a principal barreira contra uma possível infecção foi perdida. Desse modo, um curativo ideal deve suprir a função da barreira cutânea, criando uma barreira física e, consequentemente, controlando a infecção9. Além disso, deve preferencialmente auxiliar na remoção de tecidos desvitalizados, por meio de desbridamento autolítico, enzimático, mecânico ou biológico16.
A possível necrose de tecidos adjacentes pode ocorrer nas horas e dias subsequentes ao trauma e, portanto, a gestão dessa área, por meio da melhoria do fluxo sanguíneo, a modulação da inflamação e o fornecimento de um ambiente propício à sobrevivência celular, com o controle do crescimento bacteriano e o estímulo ao crescimento de queratinócitos, torna-se o alvo principal de novos tratamentos7.
Já na fase de proliferação celular, o curativo ideal deve, além de absorver o exsudato excessivo, promover um ambiente úmido, essencial para a atividade celular e para a redução da dor e a formação de tecido de granulação, facilitando a reepitelização16. Segundo Ji et al.8, a utilização de adjuvantes para acelerar a cicatrização, como fatores de crescimento de fibroblastos (FGF), fatores de crescimento epidérmico (EGF) e fatores estimuladores de colônias de granulócitos-macrófagos humanos recombinantes (rhGM-CSF), é recomendada com nível de evidência moderado.
Conforme Cook et al.1, o curativo também deve aderir ao tecido, mas ser facilmente removido e recolocado sem promover dor, possuir estabilidade mecânica, além de ter baixo custo. Ainda de acordo com os autores, futuras pesquisas devem procurar desenvolver curativos que otimizem a entrega de agentes anti-inflamatórios, pró-angiogênicos e antibióticos encapsulados ou a administração combinada de dois ou mais agentes.
Os principais microrganismos causadores de infecções em feridas por queimaduras são: Bactérias gram-positivas, como Staphylococcus aureus e Enterococcus spp.; Bactérias gram-negativas, como Pseudomonas aeruginosa, Escherichia coli, Klebsiella pneumoniae, Serratia marcescens, Enterobacter spp., Proteus spp., Acinetobacter spp. e Bacteroides spp.; Fungos, incluindo Candida spp., Aspergillus spp., Fusarium spp., Alternaria spp., Rhizopus spp. e Mucor spp.; e os vírus Herpes simplex, Cytomegalovirus e Varicella-zoster17.
Espécies Reativas de Oxigênio (EROs), que incluem radicais como o hidroxila e o ânion superóxido, em concentrações fisiológicas atuam como moléculas de sinalização essenciais, facilitando etapas críticas da cicatrização, inclusive estimulando a angiogênese18. No entanto, devido à biocarga bacteriana da ferida, há produção de grandes quantidades de EROS19. Quando a capacidade antioxidante do tecido é excedida, o estresse oxidativo resultante causa danos teciduais e apoptose, destruindo proteínas da matriz extracelular e lipídios da membrana celular, o que perpetua o ciclo inflamatório18. Isso justifica a necessidade de um composto antioxidante em curativos para queimaduras.
Por fim, além dessas propriedades, Op 't Veld et al.20 acrescentam que um curativo ideal deve promover uma cicatrização não fibrótica e sem reações inflamatórias (ser biocompatível), permitir trocas gasosas, garantir isolamento térmico, ser estéril e possuir boa moldabilidade e maneabilidade.
Membrana nanocompósita multifuncional proposta
A análise da literatura sobre os desafios dos tratamentos utilizados no presente e as propriedades de um curativo ideal demonstra a necessidade da busca por biomateriais que, em conjunto, apresentem as características de um curativo que supra as lacunas terapêuticas atuais. Estudos recentes sugerem o potencial de uma membrana nanocompósita multifuncional como possível alternativa, por meio da sinergia entre as propriedades físico-químicas, biocompatíveis, bioativas e de baixo custo entre o PVA, as NFCs e o TA. Os materiais foram selecionados com base em evidências experimentais e clínicas disponíveis na literatura, que demonstram seu desempenho em contextos de regeneração da pele.
Álcool polivinílico (PVA)
O PVA é um polímero sintético, de baixo custo, biodegradável, solúvel em água, não tóxico, não cancerígeno, não mutagênico e biocompatível. Apesar de possuir boa elasticidade e flexibilidade, o PVA possui baixa resistência mecânica e carece de propriedades antibacterianas2. Hidrogéis de PVA também são amplamente utilizados em sistemas de entrega de fármacos (drug delivery), porém podem apresentar uma liberação inicial rápida indesejada6. Além disso, a característica hidrofílica do PVA, apesar de ser capaz de manter um ambiente úmido na ferida, pode levar ao acúmulo de água em lesões com grande quantidade de exsudato, o que pode favorecer infecções bacterianas21.
Para contornar alguns desses desafios, o PVA pode passar por um processo de reticulação, que pode aumentar a resistência mecânica e retardar a liberação inicial de fármacos, tornando-a mais controlada e previsível6.
Nanofibrilas de celulose (NFCs)
A celulose (C6H10O5) derivada da madeira é o biopolímero mais abundante em nosso planeta. É sustentável, biorrenovável, acessível, de baixo custo e biocompatível. Segundo Ahmed et al., estudos de citotoxicidade in vivo e in vitro demonstraram que as nanofibrilas de celulose não representam um risco significativo para as células, apresentando baixa toxicidade. De forma similar, ainda segundo os autores, membranas de nanocelulose de madeira não provocaram reação alérgica ou resposta inflamatória. Estudos in vivo com curativos contendo nanocelulose e ácido tânico demonstram uma contração da ferida significativamente mais rápida em comparação à ausência de tratamento, com a presença da nanocelulose, em particular, resultando em uma densidade maior de fibroblastos na derme22,23.
Devido às suas boas propriedades mecânicas, a nanocelulose é considerada um excelente material de reforço. Pesquisas demonstraram que filmes de PVA com NFC apresentaram maior resistência à tração em comparação com o filme de PVA puro, apesar de apresentarem maior rigidez e uma redução na flexibilidade3,4. A combinação com o PVA também resulta em um material translúcido, propriedade comprovada em lentes de contato amplamente utilizadas, feitas com os mesmos componentes24.
A nanocelulose possui ótima capacidade de intumescimento, e com isso, tem grande capacidade de absorver exsudatos3. Contudo, a adição de derivados da celulose a compostos poliméricos reduz proporcionalmente a taxa de absorção de líquidos e a permeabilidade à água25-27, o que permite a modulação da absorção de fluidos.
Além dessa gestão de umidade, a estrutura nanométrica cria uma barreira física densa e eficaz contra a penetração de microrganismos. Essa mesma estrutura permite a passagem de gases essenciais como o oxigênio, promovendo a respiração tecidual28.
Ácido tânico (TA)
O ácido tânico (TA), um polifenol natural de baixo custo encontrado em várias plantas, atua como um agente reticulante eficaz para o PVA, por meio de ligações de hidrogênio. A adição de TA a filmes de PVA melhora significativamente propriedades como a tensão suportada e a elasticidade. Nesse tipo de sistema, o TA confere ao material importantes características antioxidantes, antimicrobianas e antibacterianas devido aos seus grupos polifenólicos4.
A ação antibacteriana do ácido tânico pode ser explicada pela capacidade de atravessar a parede celular do patógeno, interferindo em seu metabolismo e prevenindo a colonização bacteriana. O TA apresenta ótima atividade antimicrobiana contra bactérias Gram-positivas, como Staphylococcus aureus e Enterococcus faecalis, e bactérias Gram-negativas, como Escherichia coli e Pseudomonas aeruginosa, apesar de possuir um efeito mais lento contra essas29.
Conforme observado por Karakus et al.2, a introdução do TA em um hidrogel de PVA pode, inicialmente, ser capaz de reter água de forma mais eficaz em comparação com um hidrogel não reticulado. Entretanto, o aumento progressivo da concentração de TA leva a uma maior densidade de reticulação, que acaba diminuindo a capacidade de absorção de água do composto.
Um material autorregenerativo (self-healing) é caracterizado por sua capacidade de se reparar espontaneamente após ser danificado, como em casos de ruptura5. A estrutura de um compósito autorregenerativo pode ser usada para controlar a taxa de liberação de fármacos ou outros agentes bioativos, já que sua regeneração pode impedir o vazamento desses agentes, garantindo uma entrega eficaz e direcionada30. O estudo de Huang et al.5 concluiu que o ácido tânico (TA) concede 87% de eficiência autorregenerativa a um hidrogel de PVA.
DISCUSSÃO
A síntese dos dados revisados permite traçar a estrutura da membrana nanocompósita multifuncional proposta no presente trabalho, representada na Figura 1. Considerando a comparação apresentada na Tabela 1, esta estrutura teórica demonstra potencial para suprir as lacunas dos tratamentos atuais para queimaduras.
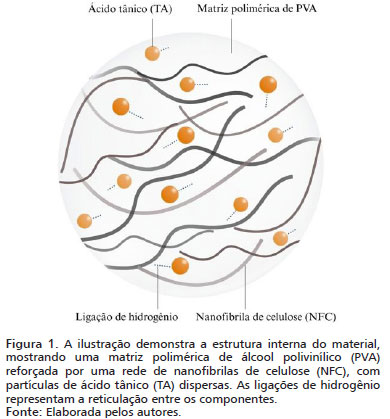
A formulação, cujo mecanismo esperado está esquematizado na Figura 2, cria um material que é capaz de gerenciar altos volumes de exsudato, através da alta capacidade de absorção das nanofibrilas de celulose (NFC), ao mesmo tempo que é resistente e possui a capacidade de autorregeneração, além de criar um sistema de liberação controlada e sustentada de fármacos, possibilitando aplicações terapêuticas personalizadas, propriedades que nenhum curativo atual apresenta simultaneamente, de acordo com a análise da Tabela 1. Clinicamente, essas características resultariam em uma menor frequência de trocas e, consequentemente, a redução da dor para o paciente e da necessidade de procedimentos sob anestesia, otimizando o tempo da equipe profissional e os recursos do centro cirúrgico.
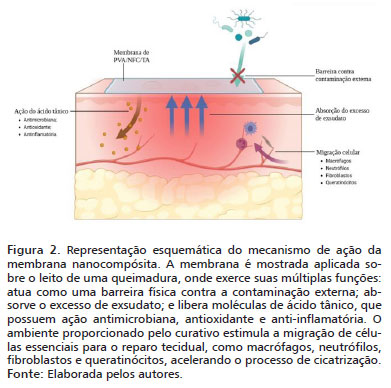
Além disso, a proposta atual, ao incorporar o ácido tânico, confere um espectro de bioatividade ao material com menor risco de citotoxicidade em comparação a agentes como a prata, amplamente utilizada em queimaduras devido à sua comprovada eficácia bactericida e bacteriostática. Essa bioatividade, somada à capacidade da celulose de estimular a migração e proliferação celular, pode, com base na presente revisão da literatura, acelerar a cicatrização de feridas por queimaduras.
Por utilizar a celulose extraída de madeira, apresenta baixo custo, além de ser mecanicamente robusta. Também funciona como barreira protetora contra microrganismos, enquanto permite as trocas gasosas essenciais e mantém um ambiente úmido, característica intrínseca da matriz de álcool polivinílico (PVA). Curativos biológicos avançados, como a pele de tilápia e a celulose bacteriana, não conseguem, atualmente, conciliar essas qualidades. É neste cenário que a presente membrana nanocompósita é proposta como opção projetada para superar as lacunas terapêuticas atuais.
Desafios e perspectivas futuras
Apesar do embasamento teórico apresentado ao longo desta revisão, a transição desta plataforma do conceito para a clínica depende da superação de alguns desafios.
A literatura indica que a introdução de NFCs, apesar de conferir maior resistência à tração ao PVA, pode aumentar a rigidez do material. Um dos primeiros desafios experimentais futuros será, assim, encontrar o equilíbrio entre a concentração de NFCs para, além de adquirir a propriedade absortiva da celulose, manter a resistência mecânica e, ao mesmo tempo, preservar a flexibilidade necessária para a adaptação do curativo ao leito da ferida. Além disso, a modulação do intumescimento em compostos poliméricos por meio da adição de NFCs também precisa ser considerada, para que o compósito absorva o excesso de exsudato da ferida sem promover uma saturação que levaria à maceração do tecido, mantendo o equilíbrio de umidade ideal para a cicatrização.
Da mesma forma, a reticulação do PVA com ácido tânico (TA) é essencial para a estabilidade e as propriedades antimicrobianas. Contudo, a literatura indica que a concentração de TA influencia diretamente na capacidade de absorção de água do composto. A determinação da proporção ideal entre PVA e TA e a avaliação da concentração mínima de TA para que seja possível garantir a eficácia de sua ação antimicrobiana e a capacidade de autorregeneração serão passos importantes para garantir a gestão eficaz do exsudato sem comprometer a ação reticulante do TA. Além disso, a reticulação não deve interferir na transparência do curativo, essencial para monitoramento clínico sem remoção.
Portanto, embora os dados revisados sustentem a viabilidade teórica da membrana PVA/NFC/TA, o presente estudo não representa validação experimental, mas uma fundamentação conceitual que poderá orientar pesquisas futuras. A continuidade deste trabalho por meio de testes experimentais detalhados é uma etapa indispensável para validar o potencial terapêutico deste material e avançar em direção a uma nova era no tratamento de queimaduras.
CONCLUSÕES
A revisão da literatura realizada evidencia que, apesar dos avanços, o tratamento de queimaduras ainda enfrenta desafios significativos, com terapias atuais muitas vezes ineficazes, desconfortáveis para o paciente e de alto custo. Considerando as lacunas dos tratamentos correntes, propõe-se teoricamente uma membrana que combinaria a capacidade de manutenção de um ambiente úmido e a flexibilidade do álcool polivinílico (PVA), a resistência mecânica e a alta capacidade de absorção das nanofibrilas de celulose (NFCs) e as propriedades reticulantes, antimicrobianas e antioxidantes do ácido tânico (TA). A proposta poderia contribuir para a aceleração do processo de cicatrização com maior segurança e controle, minimizando a frequência de trocas de curativo e, potencialmente, reduzindo o tempo de internação e os custos associados ao tratamento. Embora os dados dos estudos revisados sustentem a plausibilidade teórica da composição PVA/NFC/TA, é necessária a reprodução prática e experimental da membrana, a fim de realizar estudos in vitro e in vivo para validar sua real eficácia clínica e segurança.
PRINCIPAIS CONTRIBUIÇÕES
• Revisão crítica dos tratamentos atuais para queimaduras, evidenciando limitações clínicas e terapêuticas relevantes.
• Fundamentação teórica da proposta de uma membrana bioativa composta por PVA, NFC e TA, com propriedades sinérgicas.
• Proposta conceitual de um modelo de curativo potencialmente multifuncional, com ação antimicrobiana, antioxidante e autorregenerativa.
• Indicação de perspectivas experimentais para validação físico-química e clínica da formulação proposta.
REFERÊNCIAS
1. Cook KA, Martinez-Lozano E, Sheridan R, Rodriguez EK, Nazarian A, Grinstaff MW. Hydrogels for the management of second-degree burns: currently available options and future promise. Burns Trauma. 2022;10:tkac047.
2. Karakus NR, Türk S, Guney Eskiler G, Syzdykbayev M, Appazov NO, Özacar M. Investigation of tannic acid crosslinked PVA/PEI-based hydrogels as potential wound dressings with self-healing and high antibacterial properties. Gels. 2024;10(11):682.
3. Oprica GM, Panaitescu DM, Lixandru BE, Usurelu CD, Gabor AR, Nicolae CA, et al. Plant-derived nanocellulose with antibacterial activity for wound healing dressing. Pharmaceutics. 2023;15(12):2672.
4. Osolnik U, Vek V, Korosec RC, Oven P, Poljansek I. Integration of wood-based components - Cellulose nanofibrils and tannic acid - into a poly(vinyl alcohol) matrix to improve functional properties. Int J Biol Macromol. 2024;256(Pt 2):128495.
5. Huang J, Wu C, Yu X, Li H, Ding S, Zhang W. Biocompatible autonomic self-healing PVA-TA hydrogel with high mechanical strength. Macromol Chem Phys. 2021;222(13):2100061.
6. Rahman Khan MM, Rumon MMH. Synthesis of PVA-Based Hydrogels for Biomedical Applications: Recent Trends and Advances. Gels. 2025;11(2):88.
7. Lopes DC, Ferreira ILG, Adorno J. Manual de queimaduras para estudantes. Brasília: Sociedade Brasileira de Queimaduras; 2021.
8. Ji S, Xiao S, Xia Z; Chinese Burn Association Tissue Repair of Burns and Trauma Committee, Cross-Straits Medicine Exchange Association of China. Consensus on the treatment of second-degree burn wounds (2024 edition). Burns Trauma. 2024;12:tkad061.
9. Bukatuka CF, Mbituyimana B, Xiao L, Qaed Ahmed AA, Qi F, Adhikari M, et al. Recent Trends in the Application of Cellulose-Based Hemostatic and Wound Healing Dressings. J Funct Biomater. 2025;16(5):151.
10. Alberts A, Moldoveanu ET, Niculescu AG, Grumezescu AM. Hydrogels for wound dressings: applications in burn treatment and chronic wound care. J Compos Sci. 2025;9(3):133.
11. Saghazadeh S, Rinoldi C, Schot M, Kashaf SS, Sharifi F, Jalilian E, et al. Drug delivery systems and materials for wound healing applications. Adv Drug Deliv Rev. 2018;127:138-66.
12. Weller CD, Team V, Sussman G. First-line interactive wound dressing update: a comprehensive review of the evidence. Front Pharmacol. 2020;11:155.
13. Souza SC, Briglia C, Mendonça M. Use of polyurethane foam dressings on skin graft donor sites. Rev Bras Cir Plást. 2014;29(1):136-41.
14. Alves APNN, Verde MEQL, Ferreira Júnior AEC, Silva PGB, Feitosa VP, Lima Júnior EM, et al. Avaliação microscópica, estudo histoquímico e análise de propriedades tensiométricas da pele de tilápia do Nilo. Rev Bras Queimaduras. 2015;14(3):203-10.
15. Miranda MJB, Brandt CT. Nile tilapia skin xenograft versus silver-based hydrofiber dressing in the treatment of second-degree burns in adults. Rev Bras Cir Plást. 2019;34(1):79-85.
16. Rossi LA, Menezez MAJ, Gonçalves N, Ciofi-Silva CL, Farina-Junior JA, Stuchi RAG. Cuidados locais com as feridas das queimaduras. Rev Bras Queimaduras. 2010;9(2):54-9.
17. Church D, Elsayed S, Reid O, Winston B, Lindsay R. Burn wound infections. Clin Microbiol Rev. 200619(2):403-34.
18. Huang C, Dong L, Zhao B, Lu Y, Huang S, Yuan Z, et al. Anti-inflammatory hydrogel dressings and skin wound healing. Clin Transl Med. 2022;12(11):e1094.
19. Greaves NS, Ashcroft KJ, Baguneid M, Bayat A. Current understanding of molecular and cellular mechanisms in fibroplasia and angiogenesis during acute wound healing. J Dermatol Sci. 2013;72(3):206-17.
20. Op 't Veld RC, Walboomers XF, Jansen JA, Wagener FADTG. Design Considerations for Hydrogel Wound Dressings: Strategic and Molecular Advances. Tissue Eng Part B Rev. 2020;26(3):230-48.
21. Xu R, Fang Y, Zhang Z, Cao Y, Yan Y, Gan L, et al. Recent Advances in Biodegradable and Biocompatible Synthetic Polymers Used in Skin Wound Healing. Materials (Basel). 2023;16(15):5459.
22. Taheri P, Jahanmardi R, Koosha M, Abdi S. Physical, mechanical and wound healing properties of chitosan/gelatin blend films containing tannic acid and/or bacterial nanocellulose. Int J Biol Macromol. 2020;154:421-32.
23. Ahmed R, Das S, Banerjee J, Samanta S, Dash SK, Pramanik A. Use of nanocellulose as drug carriers for drug delivery applications. In: Mukhopadhyay M, Bhattacharya D, eds. Nanocellulose: a biopolymer for biomedical applications. John Wiley & Sons; 2024. p. 221-65.
24. Dutta G, Dastidar DG, Sugumaran A. Use of nanocellulose hydrogels for ophthalmic applications. In: Mukhopadhyay M, Bhattacharya D, eds. Nanocellulose: a biopolymer for biomedical applications. John Wiley & Sons; 2024. p. 319-34.
25. Gentile G, Cocca M, Avolio R, Errico ME, Avella M. Effect of microfibrillated cellulose on microstructure and properties of poly(vinyl alcohol) foams. Polymers. 2018;10(8):813.
26. Saha B, Mukhopadhyay M. A cutting edge biopolymer - an overview. In: Mukhopadhyay M, Bhattacharya D, eds. Nanocellulose: a biopolymer for biomedical applications. John Wiley & Sons; 2024. p. 1-26.
27. Adak S. Development of nanocellulose-based nanocomposites and its properties. In: Mukhopadhyay M, Bhattacharya D, eds. Nanocellulose: a biopolymer for biomedical applications. John Wiley & Sons; 2024. p. 113-40.
28. Poonguzhali R, Basha SK, Kumari VS. Synthesis and characterization of chitosan-PVPnanocellulose composites for in-vitro wound dressing application. Int J Biol Macromol. 2017;105(Pt 1):111-20.
29. Kaczmarek B. Tannic Acid with Antiviral and Antibacterial Activity as A Promising Component of Biomaterials-A Minireview. Materials (Basel). 2020;13(14):3224.
30. Devi VKA, Shyam R, Palaniappan A, Jaiswal AK, Oh TH, Nathanael AJ. Self-Healing Hydrogels: Preparation, Mechanism and Advancement in Biomedical Applications. Polymers (Basel). 2021;13(21):3782.
Recebido em
16 de Julho de 2025.
Aceito em
30 de Outubro de 2025.
Local de realização do trabalho: Universidade Federal do Tocantins, Medicina, Palmas, TO, Brasil.
Conflito de interesses: Os autores declaram não haver.