
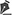
Camila Barroso Martins1; Edmar Maciel Lima Júnior2; Carlos Roberto Koscky Paier3; Eleicy Nathaly Mendoza Hernandez4; Francisco Raimundo Silva Junior5; Adelânia Roque Marinho Guedes6; Manoel Odorico de Moraes Filho7; Felipe Augusto Rocha Rodrigues8
DOI: 10.5935/2595-170X.20230009
RESUMO
OBJETIVO: Produzir um scaffold baseado em matriz extracelular (SMEC) biocompatível, atóxico e estéril, para tratamento de queimaduras e feridas. Explorou-se a utilização da pele de tilápia como alternativa, ressaltando suas propriedades semelhantes à pele humana e sua aplicação bem-sucedida em diferentes áreas médicas.
MÉTODO: Descreve o processo de preparação dos SMEC de pele de tilápia, incluindo etapas de desengorduramento, descontaminação, descelularização e irradiação por raios gama a 25kGy para esterilização. São realizados testes laboratoriais para avaliar a toxicidade celular in vitro pelo método do MTT, análises histológicas com coloração de hematoxilina-eosina, análises microbiológicas e de quantificação de DNA.
RESULTADOS: Destacam que os SMEC produzidos foram descelularizados de maneira eficaz, preservando a matriz extracelular e mostrando-se não citotóxicos. Além disso, a análise microbiológica evidenciou a esterilidade dos materiais após a irradiação, comprovando sua adequação para aplicação clínica. A quantificação de DNA revelou a efetividade da descelularização, reduzindo significativamente o conteúdo de DNA original do tecido.
CONCLUSÕES: Foi possível o desenvolvimento de uma matriz oriunda da pele de tilápia, sendo ela não citotóxica, estéril, portadora de morfologia adequada para aplicação clínica e acelular. Assim, contribuindo para inovação da ciência brasileira.
Palavras-chave: Derme Acelular. Materiais Biocompatíveis. Tilápia. Engenharia Tecidual. Ferimentos e Lesões.
ABSTRACT
OBJECTIVE: To produce a biocompatible, non-toxic, and sterile scaffold based on extracellular matrix (ECM) for the treatment of burns and wounds. The utilization of tilapia skin was explored as an alternative, highlighting its similar properties to human skin and its successful application in different medical areas.
METHODS: The process of preparing tilapia skin-derived ECM scaffolds is described, including steps of degreasing, decontamination, decellularization, and gamma ray irradiation at 25kGy for sterilization. Laboratory tests were conducted to assess in vitro cellular toxicity using the MTT method, histological analyses with hematoxylin-eosin staining, microbiological analyses, and DNA quantification.
RESULTS: It is emphasized that the produced ECM scaffolds were effectively decellularized, preserving the extracellular matrix and demonstrating non-cytotoxicity. Furthermore, microbiological analysis evidenced the sterility of the materials after irradiation, confirming their suitability for clinical application. DNA quantification revealed the effectiveness of decellularization, significantly reducing the original DNA content of the tissue.
CONCLUSIONS: The development of a tilapia skin-derived matrix was achieved, which is non-cytotoxic, sterile, possesses suitable morphology for clinical application, and is acellular. Thus, contributing to the innovation of Brazilian science.
Keywords: Acellular Dermis. Biocompatible Materials. Tilapia. Tissue Engineering. Wounds and Injuries.
INTRODUÇÃO
A pele é o maior órgão do corpo humano, compõe aproximadamente 15% do peso corpóreo e cobre uma área entre 1,5 a 2m2, em um indivíduo adulto. Possui várias funções, umas das principais é a proteção, funciona como uma barreira contra microrganismos indesejados, perdas de líquidos em excesso, promovendo o controle tegumentar e eletrolítico1.
As queimaduras são lesões causadas por danos cutâneos, ocorrem por agentes térmicos, químicos e elétricos, rompem a continuidade da pele, destruindo a primeira barreira do organismo contra agentes infecciosos, além de alterar a homeostase hidroeletrolítica, ocasionando danos à saúde e à qualidade de vida das pessoas queimadas. O grau de comprometimento está relacionado à extensão e à profundidade da queimadura, sendo classificadas em primeiro grau, acometendo somente a epiderme; segundo grau, envolve a epiderme e parcialmente a derme; e terceiro grau, atingindo todas as camadas da pele. No Brasil, a cada ano ocorrem um milhão de queimaduras, e apenas 10% procuram atendimento hospitalar; destes, 2.500 casos vão a óbito em consequência as lesões, de forma direta ou indireta2.
Existem muitos produtos no mercado direcionados ao tratamento de lesões em suas fases de cicatrização. Dentre eles, os scaffolds baseados em matriz extracelular (SMEC), que são biomateriais amplamente utilizados em países desenvolvidos, devido às vantagens e aos bons resultados3. Desde 2015, a pele de tilápia vem sendo estudada como um biomaterial alternativo, em razão da similaridade histológica com a pele humana, o alto teor de colágeno e a alta resistência mecânica4,5.
A pele de tilápia liofilizada já foi utilizada com muito sucesso no tratamento de queimaduras, na ginecologia (em vaginoplastias), na redesignação sexual, na reconstrução de dedos na Síndrome de Apert, na odontologia e na veterinária, dentre outras áreas6,7. Os resultados promissores impulsionaram o desenvolvimento de novos biomateriais como o SMEC para seu uso em lesões por queimaduras, vislumbrando novos horizontes como um dispositivo biomédico.
Na produção dos SMEC, as células nativas da pele da tilápia e seu material genético são seletivamente eliminados da matriz extracelular para produzir um biomaterial com características estruturais, bioquímicas e biomecânicas semelhantes às do tecido original. Igualmente, o biomaterial deve ser biocompatível, seguindo a normativa ISO 10993-5:2012.
Existem biomateriais no mercado internacional, derivados de pele humana (por exemplo: Graft Jacket®, Allograft®), pele porcina (por exemplo: EZ Derm®, Permacol®), submucosa intestinal porcina (por exemplo: Surgisis®) e outros. No Brasil, poucas empresas produzem SMEC, a maioria das empresas produtoras de curativos biológicos são estrangeiras, portanto, seus produtos chegam ao Brasil como itens de alto custo, devido ao grande valor agregado e aos impostos de importação.
A pele de tilápia, hoje tratada como subproduto de descarte da indústria de alimentos, é uma matéria-prima amplamente disponível, o que contribuirá para reduzir custos de produção do SMEC de pele de tilápia, e poderá concorrer em qualidade e preço com os demais produtos do mercado nacional e internacional, tornando-o mais acessível aos consumidores.
Estes dados, além dos resultados satisfatórios do uso clínico da pele da tilápia, e suas características semelhantes à estrutura morfológica da pele humana, apresentando derme composta por feixes de colágeno compactados, justificam o desenvolvimento do SMEC. Igualmente, as propriedades histológicas e mecânicas da pele da tilápia fazem com que os SMEC sejam muito promissores, assim como seu uso para reparo de lesões. O objetivo deste estudo foi produzir um SMEC biocompatível, atóxico e estéril, para tratamento de queimaduras e feridas. Explorou-se a utilização da pele de tilápia como alternativa, ressaltando suas propriedades semelhantes à pele humana e sua aplicação bem-sucedida em diferentes áreas médicas.
MÉTODO
Tipo de estudo e local da pesquisa
Trata-se de um estudo do experimental in vitro desenvolvido no Núcleo de Pesquisa e Desenvolvimento de Medicamentos da Universidade Federal do Ceará (NPDM/UFC), localizado na cidade de Fortaleza, CE. As peles foram obtidas de tilápias do Nilo e doadas pela empresa Bomar Pescados (Itarema, CE, Brasil).
Após o abate, as peles foram retiradas de forma mecânica, submetidas a lavagem em água corrente, armazenadas em frascos plásticos estéreis, previamente resfriadas (4-8ºC) em isopor contendo placas de gelo, monitorização realizada com termômetro digital interno para o transporte com duração média de 3 horas até o laboratório de cicatrização do NPDM. No laboratório foi realizada a limpeza, por meio da raspagem para retirada de músculos e escamas aderidas. Em seguida, foram lavadas com solução fisiológica estéril em temperatura ambiente e congeladas a -80ºC para conservação (não foi adicionada solução para não formação de cristais) e armazenamento até o processo final (por até 6 meses).
Preparo da matriz dérmica acelular
Foram realizados testes com soluções desengordurantes, descontaminantes e descelularizantes para a determinação do melhor protocolo, em que as estruturas morfológicas da pele de tilápia fossem preservadas e os melhores níveis de descelularização fossem alcançados. A pele foi recortada no tamanho de 4x3cm (12cm2) e armazenada a -80ºC para conservação, o descongelamento foi realizado em banho-maria a 37ºC no dia do processo. O protocolo de produção dos scaffolds de pele de tilápia foi definido em várias etapas, conforme descrito na Patente BR1020190239654A2:
1ª Etapa: as frações de pele foram inseridas em frascos de vidro estéril, adicionada solução desengordurante não estéril, as peças foram incubadas em agitador com velocidade constante de 50 a 250 rotações por minuto (rpm), a temperatura de 15 a 35ºC por 10-40 minutos.
2ª Etapa: as peles foram enxaguadas e incubadas com água ultrapura estéril em agitador com velocidade constante de 50 a 250rpm, a temperatura de 15 a 35ºC por 10-40 minutos.
3ª Etapa: adicionada solução descontaminante, em seguida enxaguadas e incubadas com água ultrapura estéril em agitador com velocidade constante de 50 a 250rpm, a temperatura de 15 a 35ºC por 10-40 minutos para retirada da solução.
4ª Etapa (descelularização): após o processo de descontaminação foi adicionada solução de descelularização. SMEC 1 foi feito com solução de surfactante não iônico e SMEC 2 com solução de detergente zwitteriônico, e incubada as amostras em agitador com velocidade constante de 50 a 250rpm, a temperatura de 15 a 35ºC por intervalo de 2 a 5 horas. Logo em seguida, foi realizado enxágue com água ultrapura estéril.
5ª Etapa: foi adicionado tampão estéril (PBS) pH 6,0 – 8,0, contendo soluções enzimáticas, incubadas em agitador com velocidade constante de 50 a 250rpm, a temperatura de 15 a 35ºC por 1-3 horas.
6ª Etapa: descartada a solução anterior, foi adicionada solução de detoxificação e incubadas em agitador com velocidade constante de 50 a 250rpm, a temperatura de 15 a 35ºC por 10-30 minutos. Após, procedeu-se a raspagem para retirada de melanóforos.
7ª Etapa: retirada a solução anterior e adicionado tampão estéril PBS pH 7,5 com adição de sais minerais e incubadas em agitador com velocidade constante de 50 a 250rpm, a temperatura de 15 a 35ºC por 1-3 horas.
8ª Etapa: Os SMEC foram congelados a -80ºC por 12-36 horas. Retirados congelados e liofilizados em aparelho Liotop 108 (Liobrás – São Carlos – SP), embalados a vácuo em dupla embalagem (ambiente não estéril), identificados com indicadores circulares de radiação, data de produção e lote para o controle de qualidade do biomaterial. Algumas amostras armazenadas sem irradiação e outras enviadas para irradiação por raios gama (Irradiador multipropósito) entre 25 e 50kGy no Instituto de Pesquisas Energéticas e Nucleares (IPEN). A radiosterilização foi supervisionada pela Dra. Mônica Beatriz Mathor, pesquisadora do IPEN. A diferença entre o SMEC 1 e 2 de pele de tilápia foi a diferença de solução descelularizante.
Avaliação da Toxicidade Celular in vitro pelo método do MTT
Para os testes de citotoxicidade, foi seguida a normativa internacional ISO 10993-5:2012, que descreve as orientações para testes de biocompatibilidade de dispositivos médicos em sistemas biológicos e determina um valor mínimo de 70% de viabilidade celular. Primeiramente, as amostras foram incubadas por 12 horas em PBS pH 7,4 estéril a 37ºC, posteriormente foram incubadas em meio RPMI por 24 horas a 37ºC, após este período o meio das amostras foi colocado em contato com células de fibroblasto L929 não tumorais (0,1 x 106 cel/mL) também utilizada como controle negativo (células e meio de cultura), e incubadas por 24 horas em estufa, a 37ºC e 5%. Após esse período, foi determinada a viabilidade celular pelo método do (3-4,5-dimetil-2-tiazol-2,5-difenil- brometo de tetrazólio) (MTT), usando um espectrofotômetro de placa (Beckman Coulter Inc., modelo DTX-880) no comprimento de onda de 570nm.
Análise histológica
Para a análise histológica, as frações de SMEC liofilizados foram reidratadas por 15 minutos e 16 horas, logo após foram fixadas individualmente em tubos com solução tamponada de formaldeído 10% (v/v) (pH 7,4), por 24 horas. Inicialmente, as amostras foram analisadas de forma macroscópica, por meio do exame de alterações na forma, coloração e consistência.
As lâminas histológicas foram submetidas às colorações de Hematoxilina-eosina. Para realização das análises, foi utilizado um microscópio óptico com câmera acoplada em um aumento de 200x (vezes), foram avaliadas as disposições, quantidades e a organização das fibras de colágeno dos SMEC, não houve comparação de parâmetros de normalidade.
Esses procedimentos foram executados pela equipe do Laboratório de Histopatologia do NPDM/UFC e do Laboratório de Patologia Bucal, localizado na Faculdade de Farmácia, Odontologia e Enfermagem da UFC, ambos sob coordenação da Prof.ª. Dra. Ana Paula Negreiros Nunes Alves.
Análise microbiológica
As amostras dos SMEC 1 e 2 (sem irradiação e irradiadas a 25kGy, 35kGy e 50kGy) e de pele in natura (controle negativo) foram inseridas em tubos de vidro que continham caldo BHI; em seguida, os tubos foram incubados por 24 horas em estufa bacteriológica a 35ºC, com margem de +1ºC ou –1ºC (QUIMIS, modelo Q316M4), para o enriquecimento e crescimento de possíveis microrganismos. Após a incubação, o caldo foi semeado em placa Ágar sangue (meio nutritivo e não seletivo) e incubado por 24 horas. Após 24 horas, as placas foram analisadas; se houvesse crescimento, eram incubadas por mais 24 horas, totalizando 48 horas para uma nova análise. A contagem das unidades formadoras de colônias (UFC/g) foi realizada de forma macroscópica (análise quantitativa), não sendo realizada a identificação dos microrganismos.
Extração e quantificação de DNA (úmido)
A extração de DNA da pele de tilápia in natura (controle negativo) e dos SMEC envolveu o corte de fragmentos de 50mg, seguido pela adição de uma solução contendo tampão de lise e enzima Proteinase K. Esses fragmentos foram incubados a 65ºC por 1 hora e depois submetidos a um processo de centrifugação, seguido pela adição de NaCl e isopropanol. Após uma incubação noturna a -20ºC, as amostras foram centrifugadas novamente, lavadas com etanol 70% e, por fim, o DNA foi suspenso em água destilada estéril. A concentração do DNA extraído foi avaliada utilizando um kit de ensaio de DNA em um fluorímetro Qubit. Essa técnica, adaptada de Aljanabi & Martinez8, foi empregada para estimar a quantidade de material genético presente nas amostras de pele de tilápia e dos SMEC.
Análise estatística
Os resultados foram analisados com o software GraphPad Prism®, versão 8.01 para Windows® (GraphPad Software, San Diego, California, USA, 2018). As análises estatísticas foram realizadas pelo teste de variância (ANOVA), seguido pelo pós-teste de Tukey, sendo o valor de p<0,05 considerado significante.
RESULTADOS
O estudo evidenciou a existência de facilidades na produção do SMEC de pele de tilápia, como a aquisição facilitada de matéria-prima (pele de tilápia), um produto de descarte abundante e disponível em criadores de todo o país. Adicionalmente, a existência prévia de resultados favoráveis com o curativo biológico de pele de tilápia, em diversas áreas clínico-cirúrgicas, reforçou a segurança da matéria-prima para uso médico e encorajou a proposta de desenvolvimento do novo biomaterial. No entanto, identificaram-se dificuldades, incluindo a necessidade de realizar múltiplos testes para a padronização das soluções do protocolo, a obtenção de uniformidade no tamanho e espessura dos SMEC e a correta esterilização do biomaterial.
Análise macroscópica dos SMEC de pele de tilápia
Ao final do processo, o biomaterial evidenciou uma superfície levemente acinzentada em sua derme, enquanto sua epiderme não apresentou remanescentes de melanóforos. Seu aspecto minimamente gelatinoso (antes da liofilização) e uniforme, apresentando boa resistência, não possuindo odor. Após a liofilização, os biomateriais mantêm sua coloração, apresentando uma matriz mais enrijecida e seca (Figura 1). Após serem submetidas à hidratação, a matriz retorna à maleabilidade.

Análise histológica
Foram analisados os SMEC em dois diferentes tempos de hidratação: 15 minutos e 16 horas. A análise microscópica evidenciou que o SMEC 1 apresenta feixes de colágeno, mais compactados na periferia e, centralmente, feixes esparsos e fragmentados, não foram visualizados núcleos celulares (Figura 2A, B, C, D). O SMEC 2 apresentou feixes de colágeno com compactação na superfície, seguidos por feixes esparsos e fragmentados, não havendo núcleos de células evidentes (Figura 2E, F, G, H, I). Os SMEC foram considerados materiais descelularizados e com feixes de colágeno conservados.
Análise da citotoxicidade
Os testes de citotoxicidade foram essenciais para a escolha de protocolos e aprovação dos biomateriais. Assim, em conformidade com a normativa ISO 10993-5:2012, o percentual de viabilidade celular mínimo de cada SMEC testado tem que estar acima de 70% para ser classificado como não citotóxico.
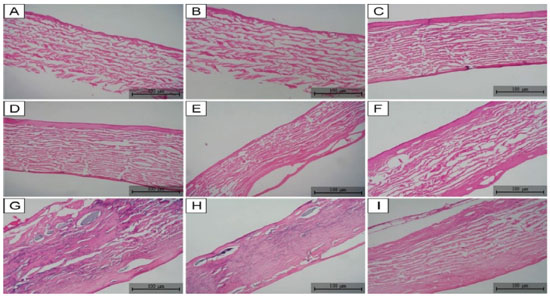
O SMEC 1 manteve a confluência e morfologia fusiforme das células L929, similares do controle negativo (células + meio). As médias e desvio padrão das viabilidades celulares obtidas em razão do contato com o extrato foram de 110,3%±3,112 (SMEC irradiado a 25kGy), 114,4%±4,607 (SMEC irradiado a 35kGy) e 110,1%±3,230 (SMEC irradiado a 50kGy). Todas as amostras foram aprovadas, de acordo com a norma ISO 10993-5:2012.
Nos ensaios com amostras de SMEC 2, a confluência das células L929 diminuiu, enquanto a morfologia celular tornou-se majoritariamente arredondada, diferente das células do controle negativo (células + meio). As viabilidades celulares alcançadas foram de 128,3%±20,11 (SMEC irradiado a 25kGy), 97,25%±2,187 (SMEC irradiado a 35kGy), resultados aprovados. O scaffold irradiado a 50kGy apresentou uma viabilidade celular de 32,23%±13,40, resultado que foi significativamente baixo em comparação ao controle. Este SMEC foi reprovado no teste de citotoxicidade.
Constatou-se que a viabilidade celular (%) do SMEC 1 em diferentes doses de irradiação (25, 30 e 50kGy) foi significativamente maior (p=0,0033) que a do controle negativo. Não foram constatadas diferenças estatisticamente significantes entre as amostras do SMEC 1 irradiadas em diferentes doses (Figura 3 (1)). Já nos ensaios do SMEC 2, não houve diferença estatística quanto às amostras irradiadas a 25 e 35kGy, comparadas ao controle. Foi evidenciada diferença significativa entre o SMEC 2 a 50kGy, comparado ao controle negativo e às demais amostras irradiadas em diferentes doses (p≤0,0001) (Figura 3 (2)).
Análise microbiológica
Nas amostras de pele in natura houve um crescimento de diferentes morfotipos, microrganismo com contagem superior a 1.000.000UFC. Já nos fragmentos sem irradiação, nos SMEC do protocolo 1, houve um crescimento inferior a 5UFC, no SMEC do protocolo 2 as amostras não apresentaram crescimento de microrganismos. Após a irradiação dos biomateriais com as doses de 25, 35 e 50kGy, não foi constatado crescimento microbiológico em nenhum dos protocolos. Foram obtidos resultados positivos do produto, totalizando 18 amostras analisadas.
Quantificação de DNA
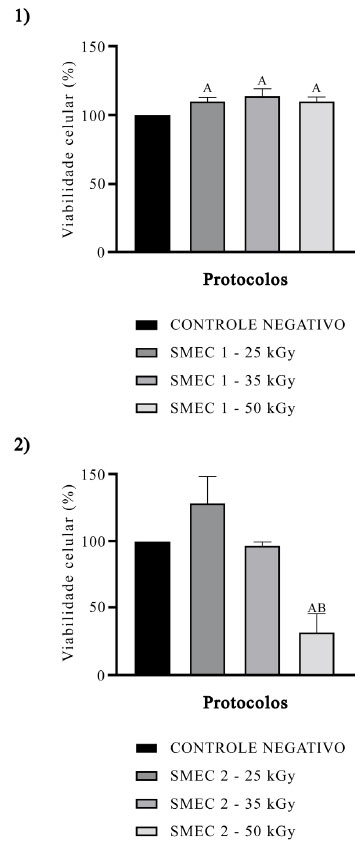
A pele de tilápia in natura teve uma quantidade de DNA de 39,21±2,14ng/mg (Média±DP), o SMEC 1 e 2 apresentaram uma diminuição de DNA ao final da descelularização, para o SMEC 1 um resultado de 2,98±0,60ng/mg (Média±DP), e para o SMEC 2 de 2,08±0,34ng/mg (Média±DP). Ambos os SMEC foram considerados estatisticamente significativos (p<0,0001) e próprios de um biomaterial descelularizado (Figura 4), havendo eliminação de mais de 50% de DNA comparado ao tecido de origem9. Assim, se confirmou que os tratamentos químicos conseguiram descelularizar de forma efetiva a pele da tilápia.
DISCUSSÃO
Estabelecer o protocolo de produção de SMEC da pele da tilápia foi um desafio, tendo em vista que existem critérios a serem seguidos, como descelularização ideal, estrutura extracelular mantida e eliminação de todas as células do tecido original10. Esses protocolos de descelularização foram realizados entre 24 a 36 horas; comparado a outros protocolos de descelularização, apresentou um menor tempo de execução. Um estudo realizado em Singapura avaliou a pele de tilápia descelularizada e evidenciou um processo com duração de 37 horas, seguido de 24 horas de liofilização e mais 1 hora na câmara a vácuo, totalizando 62 horas para produção do biomaterial11. Outro estudo em Xangai, na China, apresentou o processo tendo duração de 31 horas, porém o biomaterial não passou por processo de liofilização12.
A liofilização apresenta diversas vantagens para a preservação de biomateriais, incluindo a preservação da estrutura e função, estabilidade a longo prazo, redução da degradação térmica, minimização de danos durante a desidratação e facilidade de reidratação13. A produção de SMEC de pele de tilápia liofilizado e radioesterilizado permite o transporte a temperatura ambiente, reduz os custos e garante a esterilidade do produto.
A histologia teve como resultados, nesse estudo, uma alteração nos aspectos macroscópicos, sendo a alteração mais visível a perda de pigmentos pretos denominados melanóforos. Os cruzamentos das fibras de colágeno estavam presentes, os feixes apresentaram espaçamento, porosidade e áreas de fragmentação11. O espaço observado nas lâminas histológicas permite a regeneração da matriz extracelular (MEC), promovendo a migração de novas células, o que é importante para a implantação e, assim, remodelação e integração da MEC14.
Os protocolos de descelularização 1 e 2 modificaram feixes de fibras de colágenos da pele de tilápia em ambos os biomateriais, apresentando fragmentação no centro e mais compacta na periferia, o que se justifica devido a todo o processo químico e físico do método. Nenhum núcleo celular foi visualizado em ambos os produtos, portanto, o método de descelularização foi eficaz e a textura da pele da tilápia foi mantida em nível satisfatório.
Outro critério de avaliação para dispositivos médicos é o teste de citotoxicidade in vitro, utilizando a normativa ISO 10993-5:2012, que determina um valor mínimo de 70% de viabilidade celular, para que o material não seja considerado tóxico. Um estudo realizado com pele de tilápia descelularizada no qual foi avaliada a citotoxicidade pelo método MTT com células L929 mostrou que os protocolos estabelecidos são atóxicos, com viabilidade celular média superior a 100%, e foram considerados biomateriais aprovados para uso em medicina regenerativa12.
Os resultados da citotoxicidade nesse estudo sugerem que o SMEC 1 e 2 após a irradiação a 25kGy, 35kGy e 50kGy tiveram viabilidade celular acima de 70%, somente o SMEC 2 irradiado a 50kGy apresentou um resultado menor do que 70% de viabilidade celular. Essa amostra também proporcionou uma mudança morfológica nas células L929 em contato com seu extrato, sendo reprovada. As demais amostras irradiadas foram aprovadas com um percentual de viabilidade maior que 95%. Portanto, os SMEC 1 e 2 foram considerados biomateriais não citotóxicos.
A matéria-prima da matriz dérmica acelular de pele de tilápia provém de um animal de vida livre, em que a pele permanece em contato direto com a água do meio circundante. Dessa forma, a pele de tilápia é naturalmente exposta a uma grande diversidade de microrganismos presentes no habitat do peixe, o que exige uma criteriosa investigação dos métodos de esterilização com radiação gama, tanto da própria pele quanto dos seus produtos derivados. Os testes em diversas doses de irradiação foram realizados para comparação e padronização técnica do protocolo de desenvolvimento dos SMEC. Ao final, a irradiação a dose de 25kGy foi escolhida, pois demonstrou eficácia na esterilização, sem comprometimento significativo da estrutura microscópica do biomaterial.
O desenvolvimento de um protocolo capaz de retirar todo o material celular do tecido é essencial, assim, o potencial imunogênico é eliminado ou diminuído15. Alguns autores relatam que um tecido ou órgão é considerado acelular quando pelo menos 50% dos ácidos nucleicos e outro material celular foram removidos da matriz extracelular, em comparação com o tecido ou órgão original9. O protocolo estabelecido neste estudo conseguiu eliminar mais de 90% do DNA original do tecido, indicando uma redução no SMEC 1 de 92,39% no conteúdo de DNA; para o SMEC 2, houve uma redução de 94,69%. Isso significa uma menor chance de rejeição durante sua aplicação16.
Estes resultados foram alcançados devido à utilização de soluções detergente-enzimáticas, possibilitando a remoção completa de resíduos celulares e a degradação de ácidos nucleicos17. Pesquisas relatam que o uso de biomateriais de origem alogênica ou xenogênica requer descelularização para evitar o risco de rejeição e atividade imunogênica, como remodelamento incorreto, que é prejudicial e pode estimular a produção de citocinas pró-inflamatórias18.
Também foi necessário realizar análises microbiológicas em produtos de saúde. Esses testes são fundamentais para identificar e caracterizar os microrganismos presentes nos materiais, garantindo que sejam inofensivos para o organismo receptor.
Na pele de tilápia in natura, foram identificados mais de 110 microrganismos, sendo que os mais comuns foram os Gram-negativos. Também encontramos Gram-positivos dos gêneros Globicatella, Streptococcus e Enterococcus. Além disso, isolamos Pseudomonas aeruginosa e 24 Enterobacteriacae. É importante destacar que foi identificada a presença de Gram-positivos como o Enterococcus faecalis, que predominou em 70% das amostras de pele e da cavidade oral. Vale ressaltar que, nessa análise, a carga bacteriana foi inferior a 100.000 UFC, o que é considerado normal de acordo com os padrões estabelecidos pela Agência Nacional de Vigilância Sanitária (ANVISA)19.
Neste estudo, também foram realizados testes microbiológicos através do cultivo em placas contendo Ágar Sangue. Os procedimentos analisados após a irradiação não revelaram crescimento microbiológico, o que sugere que a desinfecção dos produtos durante a produção e a radioesterilização subsequente são eficazes. Microrganismos presentes naturalmente na pele da tilápia, em contato com qualquer tecido lesionado, podem estimular uma infecção bacteriana secundária, portanto, sempre que um biomaterial for aplicado em uma superfície lesionada, é necessário que o produto seja previamente descontaminado para torná-lo adequado ao uso20.
Este estudo identificou três limitações significativas, as quais foram: a escassez de literatura disponível sobre o processo de descelularização de pele de peixe, o que dificultou a obtenção de dados e conhecimento aprofundado sobre o assunto; a produção em baixa escala ocasionada pela dependência de mão de obra manual, que resultou em uma produção limitada e uma capacidade restrita de atender à demanda em larga escala; e o alto custo dos insumos utilizados na produção.
CONCLUSÕES
Ao final dos testes in vitro, constatou-se que os SMEC da pele de tilápia, desenvolvidos neste trabalho, foram não citotóxicos, estéreis, portadores de morfologia adequada para aplicação clínica, e acelulares, pois perderam mais de 90% do DNA do tecido original. Com base nesses resultados, conclui-se que os SMEC 1 e 2 de tilápia do Nilo são considerados biomateriais adequados, por atenderem às exigências estabelecidas para um material biocompatível.
São uma forma sustentável de biomaterial, pois utilizam como matéria-prima um subproduto de descarte da psicultura. Surgem como promissora inovação na medicina regenerativa e na ciência brasileira, suprindo necessidades clínicas dos usuários e dos profissionais de saúde, além de estimularem as empresas nacionais à produção de bens de alta tecnologia.
AGRADECIMENTOS
O presente trabalho foi realizado com apoio da Fundação Cearense de Apoio ao Desenvolvimento Científico e Tecnológico (Funcap) e Instituto de Apoio ao Queimado (IAQ).
INFORMAÇÕES FINAIS
A presente tecnologia tem pedido de patente no Brasil (BR1020190239654A2) e WIPO-PCT (WO2020097711).
REFERÊNCIAS
1. Mazurek Ł, Szudzik M, Rybka M, Konop M. Silk Fibroin Biomaterials and Their Beneficial Role in Skin Wound Healing. Biomolecules [Internet]. 2022;12(12):1852 [cited 2023 Nov 24]. Disponível em: https://www.mdpi.com/2218-273X/12/12/1852
2. Bruno PEQ, Will E, Santos GS, Felberg JS, Souza RZ. Assistência de enfermagem a pacientes com queimaduras de terceiro grau-curativos. Braz J Implant Health Sci [Internet]. 2023;5(5):1776-93 [acesso 2023 Nov 24]. Disponível em: https://bjihs.emnuvens.com.br/bjihs/article/view/750
3. Tavelli L, McGuire MK, Zucchelli G, Rasperini G, Feinberg SE, Wang HL, et al. Extracellular matrix-based scaffolding technologies for periodontal and peri-implant soft tissue regeneration. J Periodontol [Internet]. 2020;91(1):17-25 [acesso 2023 Nov 24]. Disponível em: https://aap.onlinelibrary.wiley.com/doi/10.1002/JPER.19-0351
4. Alves APNN, Verde MEQL, Ferreira Júnior AEC, Silva PGB, Feitosa VP, Lima Júnior EM, et al. Avaliação microscópica, estudo histoquímico e análise de propriedades tensiométricas da pele de tilápia do Nilo. Rev Bras Queimaduras [Internet]. 2015;14(3):203-10 [acesso 2024 Feb 8]. Disponível em: http://rbqueimaduras.org.br/details/263/pt-BR/avaliacao-microscopica--estudo-histoquimico-e-analise-de-propriedades-tensiometricas-da-pele-de-tilapia-do-nilo
5. Lima Júnior EM, Moraes Filho MO, Costa BA, Rohleder AVP, Rocha MBS, Fechine FV, et al. Innovative Burn Treatment Using Tilapia Skin as a Xenograft: A Phase II Randomized Controlled Trial. J Burn Care Res [Internet]. 2020;41(3):585-92 [acesso 2023 Nov 24]. Disponível em: https://academic.oup.com/jbcr/article/41/3/585/5695972
6. Dias MTPM, Bilhar APM, Rios LC, Costa BA, Duete UR, Lima Júnior EM, et Fish Skin as a biological graft. J Surg Case Reports [Internet]. 2019;2019(11):rjz311 [acesso 2023 Nov 24]. Disponível em: https://academic.oup.com/jscr/article/doi/10.1093/jscr/rjz311/5634096
7. Rodríguez AH, Lima Júnior EM, Moraes Filho MO, Costa BA, Bruno ZV, Monteiro Filho MP, et al. Male-to-Female Gender-Affirming Surgery Using Nile Tilapia Fish Skin as a Biocompatible Graft. J Minim Invasive Gynecol [Internet]. 2020;27(7):1474-5 [acesso 2023 Nov 24]. Disponível em: https://linkinghub.elsevier.com/retrieve/pii/S1553465020301205
8. Aljanabi S, Martinez I. Universal and rapid salt-extraction of high quality genomic DNA for PCR- based techniques. Nucleic Acids Res [Internet]. 1997;25(22):4692-3 [acesso 2023 Nov 25]. Disponível em: https://academic.oup.com/nar/article-lookup/doi/10.1093/nar/25.22.4692
9. Sigurjonsson GF, Gisladottir DH, Gudmundsson G, inventors; Kerecis EHF, assignee. Scaffold material for wound care and/or other tissue healing applications. United States Patent US 8613957 B2. 2013 Dec 24.
10. Shakouri-Motlagh A, O'Connor AJ, Brennecke SP, Kalionis B, Heath DE. Native and solubilized decellularized extracellular matrix: A critical assessment of their potential for improving the expansion of mesenchymal stem cells. Acta Biomater [Internet]. 2017;55:1-12 [acesso 2023 Nov 25]. Disponível em: https://linkinghub.elsevier.com/retrieve/pii/S1742706117302398
11. Lau CS, Hassanbhai A, Wen F, Wang D, Chanchareonsook N, Goh BT, et al. Evaluation of decellularized tilapia skin as a tissue engineering scaffold. J Tissue Eng Regen Med [Internet]. 2019;13(10):1779-91 [acesso 2023 Nov 25]. Disponível em: https://onlinelibrary.wiley.com/doi/10.1002/term.2928
12. Li D, Sun WQ, Wang T, Gao Y, Wu J, Xie Z, et al. Evaluation of a novel tilapia-skin acellular dermis matrix rationally processed for enhanced wound healing. Mater Sci Eng C [Internet]. 2021;127:112202 [acesso 2023 Nov 26]. Disponível em: https://linkinghub.elsevier.com/retrieve/pii/S0928493121003428
13. Molnar A, Lakat T, Hosszu A, Szebeni B, Balogh A, Orfi L, et al. Lyophilization and homogenization of biological samples improves reproducibility and reduces standard deviation in molecular biology techniques. Amino Acids [Internet]. 2021;53(6):917-28 [acesso 2024 Feb 8]. Disponível em: https://link.springer.com/article/10.1007/s00726-021-02994-w
14. Murphy AR, Haynes JM, Laslett AL, Cameron NR, O'Brien CM. Three-dimensional differentiation of human pluripotent stem cell-derived neural precursor cells using tailored porous polymer scaffolds. Acta Biomater [Internet]. 2020;101:102-16 [acesso 2023 Nov 26]. Disponível em: https://linkinghub.elsevier.com/retrieve/pii/S1742706119306932
15. Macagonova O, Risnic D, Cociug A, Nacu V. Comparative analysis of the skin decellularization methods. Mold Med J [Internet]. 2021;64(2):79-86 [acesso 2023 Nov 26]. Disponível em: http://moldmedjournal.md/wp-content/uploads/2021/05/moldovanmed-j-2021-64-2-macagonova-et-al-full-text.pdf
16. Kim BS, Kim H, Gao G, Jang J, Cho DW. Decellularized extracellular matrix: a step towards the next generation source for bioink manufacturing. Biofabrication [Internet]. 2017;9(3):034104 [acesso 2023 Nov 26]. Disponível em: https://iopscience.iop.org/article/10.1088/1758-5090/aa7e98
17. Zambaiti E, Scottoni F, Rizzi E, Russo S, Deguchi K, Eaton S, et al. Whole rat stomach decellularisation using a detergent-enzymatic protocol. Pediatr Surg Int [Internet]. 2019;35(1):21-7 [acesso 2023 Nov 26]. Disponível em: http://link.springer.com/10.1007/s00383-018-4372-8
18. Barreto RS, Romagnolli P, Fratini P, Mess AM, Miglino MA. Mouse placental scaffolds: a three-dimensional environment model for recellularization. J Tissue Eng [Internet]. 2019;10:204173141986796 [acesso 2023 Nov 26]. Disponível em: http://journals.sagepub.com/doi/10.1177/2041731419867962
19. Lima Junior EM, Bandeira TJPG, Miranda MJB, Ferreira GE, Parente EA, Piccolo NS, et al. Characterization of the microbiota of the skin and oral cavity of Oreochromis niloticus. J Health Biol Sci [Internet]. 2016;4(3):193-7 [acesso 2023 Nov 26]. Disponível em: https://periodicos.unichristus.edu.br/jhbs/article/view/767
20. Alves APNN, Lima Júnior EM, Piccolo NS, Miranda MJB, Verde MEQV, Ferreira Júnior AEC, et al. Study of tensiometric properties, microbiological and collagen content in nile tilapia skin submitted to different sterilization methods. Cell Tissue Bank. [Internet]. 2018 [acesso 2023 Nov 26];19(3):373-82. Disponível em: https://link.springer.com/article/10.1007/s10561-017-9681-y
Recebido em
1 de Dezembro de 2023.
Aceito em
28 de Fevereiro de 2024.
Local de realização do trabalho: Núcleo de Pesquisa e Desenvolvimento de Medicamentos da Universidade Federal do Ceará, Fortaleza, CE, Brasil.
Conflito de interesses: Os autores declaram não haver.
Trabalho vencedor do Prêmio Roberto Chem no XIII Congresso Brasileiro de Queimaduras (Salvador, BA, 27 a 29 de setembro de 2023).